
 Nederlands onderzoek uit 2019 laat zien dat minstens 36.500 mensen in ons land MS hebben, zo’n 10.000 meer dan eerdere schattingen van de Internationale MS Federatie (MSIF). MS Vereniging Nederland kwam eerder al uit op 34.000. De resultaten zijn gepubliceerd in Multiple Sclerosis and Related Disorders (Elsevier BV).
Nederlands onderzoek uit 2019 laat zien dat minstens 36.500 mensen in ons land MS hebben, zo’n 10.000 meer dan eerdere schattingen van de Internationale MS Federatie (MSIF). MS Vereniging Nederland kwam eerder al uit op 34.000. De resultaten zijn gepubliceerd in Multiple Sclerosis and Related Disorders (Elsevier BV).
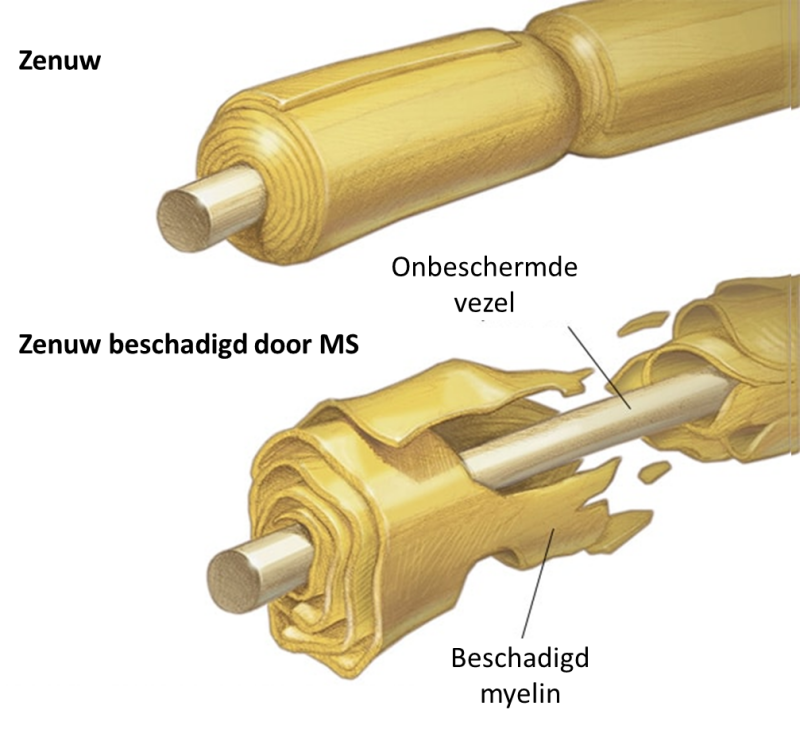
Multiple sclerose (MS) is de meest voorkomende invaliderende neurologische ziekte bij jongvolwassenen, waarbij symptomen doorgaans beginnen tussen de leeftijd van 20 en 40 jaar. Bij MS vallen cellen van het immuunsysteem die normaal gesproken ons beschermen tegen virussen, bacteriën en ongezonde cellen per abuis myeline aan in het centrale zenuwstelsel (hersenen, oogzenuwen en ruggenmerg). Myeline is een stof die de beschermende schede (myelineschede) vormt rond zenuwvezels (axonen).
De Cruciale Rol van Zenuwen bij Spierfunctie en Lichaamscontrole
Spieren hebben zenuwvoorziening nodig om te kunnen samentrekken en spanning vast te houden. Bij gewervelde dieren regelen motorneuronen dit proces door acetylcholine vrij te maken in de neuromusculaire overgang. Wanneer een actiepotentiaal (elektrische impuls) het uiteinde van een motorneuron bereikt, openen spanningsafhankelijke calciumkanalen, waardoor calcium de cel binnenstroomt. Dit calcium zorgt ervoor dat blaasjes gevuld met acetylcholine versmelten met het membraan van het neuron, waardoor acetylcholine wordt vrijgegeven.
Acetylcholine bindt aan receptoren op het spiercelmembraan (sarcolemma), wat natriumkanalen opent. Dit genereert een nieuwe actiepotentiaal in de spiercel, die zich naar de myofibrillen verplaatst en leidt tot spiercontractie.
Zowel somatische als autonome zenuwen spelen een rol in de spierfunctie. Somatische zenuwen sturen vrijwillige bewegingen aan, zoals het optillen van een arm. Autonome zenuwen regelen onvrijwillige processen zoals de contractie van spieren in de blaas of kliersecreties.
Een voorbeeld hiervan is de parasympathische zenuwinvloed op de blaas: deze zorgt ervoor dat de detrusorspier samentrekt en de interne sfincter ontspant, zodat urineren mogelijk wordt. De sympathische zenuwen doen juist het tegenovergestelde door de detrusorspier te ontspannen en de interne sfincter te vernauwen, wat urineren tegenhoudt. Bovendien speelt somatische aansturing van de externe sfincter ook een rol in dit proces.
MS ontstaat door beschadigd myeline
Multiple Sclerose (MS) is een chronische aandoening die het centrale zenuwstelsel (hersenen en ruggenmerg) aanvalt. Bij MS richt het immuunsysteem zich tegen de beschermende laag van de zenuwen, de myeline. Myeline is een vetachtige substantie die de zenuwen omhult en zorgt voor een snelle en efficiënte overdracht van elektrische signalen. Wanneer deze beschermende laag beschadigd raakt, ontstaan er communicatieproblemen tussen de hersenen en de rest van het lichaam.
Door de beschadiging van myeline ontstaat er littekenweefsel, ook wel sclerose genoemd, wat zichtbaar is als plaques of laesies. Deze plekken kunnen variëren in grootte en zijn te detecteren met een magnetische resonantiebeeldvorming (MRI). Wanneer zenuwen door deze plaques beschadigd raken, verliezen ze hun vermogen om signalen correct door te geven, wat leidt tot lichamelijke en cognitieve klachten.
Daarnaast richt MS zich niet alleen op de myeline, maar ook op de zenuwcellichamen in de grijze stof van de hersenen. De grijze stof bevat de cellichamen van de zenuwcellen en speelt een cruciale rol in cognitieve functies zoals denken, geheugen en emoties. Naarmate de ziekte vordert, kan dit ook leiden tot krimp van de hersenschors, het buitenste deel van de hersenen, in een proces dat corticale atrofie wordt genoemd.
De hersenschors bestaat uit grijze stof en is verantwoordelijk voor veel complexe cognitieve processen. Het is opgebouwd uit zes verschillende lagen, die elk een specifieke rol hebben in de verwerking van informatie. De neuronen in de hersenschors sturen signalen naar andere delen van de hersenen en het zenuwstelsel. De ondersteuning van deze neuronen wordt verzorgd door gliacellen, die zorgen voor voeding, het opruimen van afvalstoffen, en het isoleren van axonen met myeline.
Onder de hersenschors ligt de witte stof, die bestaat uit gemyeliniseerde axonen die de verschillende hersengebieden met elkaar verbinden. Deze verbindingen zijn essentieel voor de communicatie tussen de hersenen en het hele lichaam. Het netwerk van bloedvaten in de hersenen voorziet deze structuren van de benodigde zuurstof en voedingsstoffen om optimaal te functioneren.
Wanneer MS vordert, kan het leiden tot blijvende schade aan de zenuwen en zenuwvezels, wat de hersenfunctie en het dagelijks functioneren van patiënten ernstig kan beïnvloeden. De combinatie van schade aan zowel de myeline als de zenuwcellichamen maakt MS tot een complexe en ingrijpende ziekte.
Oligodendrocyten: Sleutelfunctie in Myelinisatie
Oligodendrocyten zijn de myeliniserende cellen van het centrale zenuwstelsel en vormen ongeveer 5 tot 10% van de totale gliapopulatie. Deze cellen zijn verantwoordelijk voor de productie van de myelineschede, die essentieel is voor zowel de snelle en efficiënte geleiding van elektrische impulsen langs de axonen als het behoud van axonale integriteit. Oligodendrocyten ontstaan uit oligodendrocyt-progenitorcellen die zich vermenigvuldigen en differentiëren vlak voor en na de geboorte, onder een sterk gereguleerd programma. Zowel oligodendrocyten als hun voorlopers zijn zeer vatbaar voor letsel door verschillende mechanismen, waaronder excitotoxische schade, oxidatieve stress en ontstekingsgebeurtenissen. In deze review zullen we niet alleen verschillende belangrijke aspecten van de ontwikkeling van oligodendrocyten en regulerende mechanismen die bij dit proces betrokken zijn behandelen, maar ook enkele van de belangrijkste pathways van letsel gerelateerd aan oligodendrogenese [2].
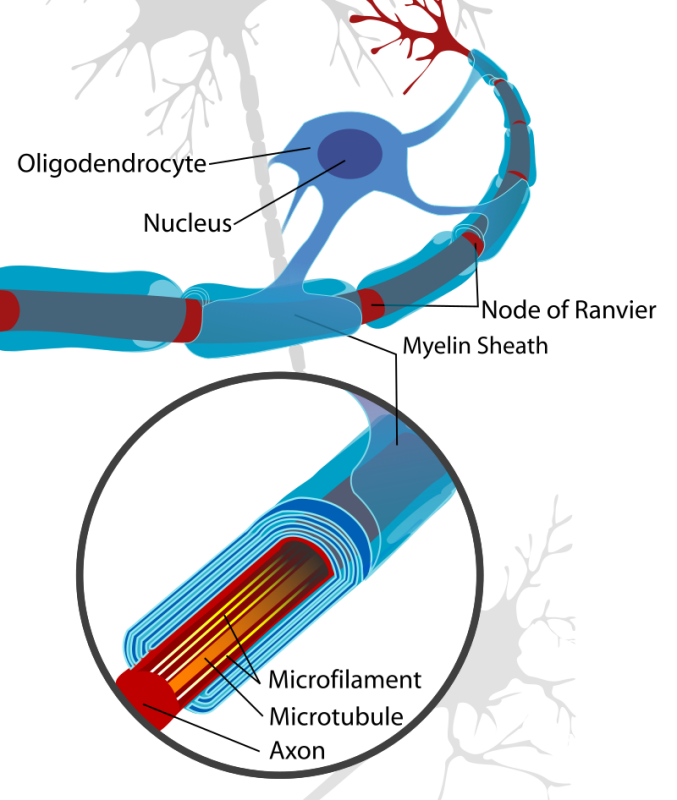
Bron: https://vm.tiktok.com/ZGd5nDbag/
Myelinisatie van axonen in het zenuwstelsel van gewervelde dieren maakt snelle, zoutatorische impulsvoortplanting mogelijk, een van de best begrepen concepten in de neurofysiologie. Het kostte echter geruime tijd om de mechanistische complexiteit van zowel myelinisatie door oligodendrocyten en Schwann-cellen als hun cellulaire interacties te erkennen. In deze review belichten we recente ontwikkelingen in ons begrip van myelinevorming, de levenslange plasticiteit ervan en de wederzijdse interacties van myelinerende gliacellen met de axonen die ze omhullen. In het centrale zenuwstelsel wordt myelinisatie ook gestimuleerd door axonale activiteit en astrocyten, terwijl myelineklaring betrokkenheid van microglia/macrophages omvat. Eenmaal gemyeliniseerd, is de langetermijnintegriteit van axonen afhankelijk van de levering van metabolieten en neurotrofe factoren door gliacellen. De relevantie van deze axogliale symbiose wordt geïllustreerd in normale veroudering van de hersenen en menselijke myelineziekten, die kunnen worden bestudeerd in overeenkomstige muismodellen. Zo spelen myeliniserende cellen een sleutelrol bij het behouden van de connectiviteit en functies van een gezond zenuwstelsel [3].
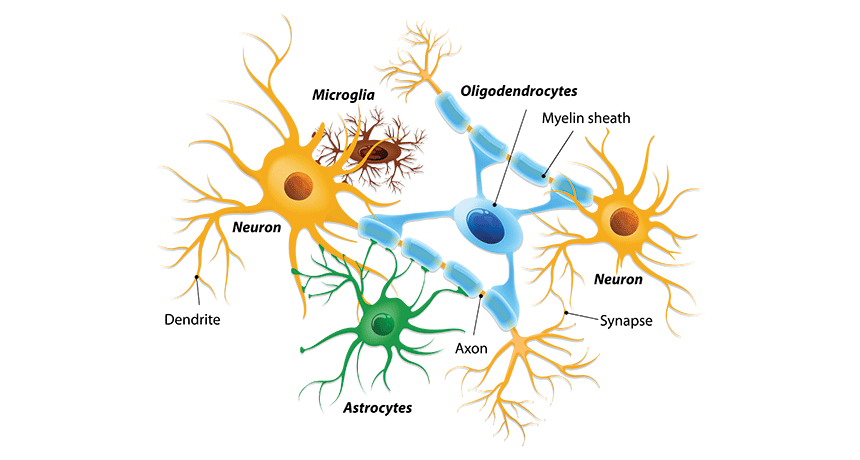 Oligodendrocyten zijn de myeliniserende cellen van het centrale zenuwstelsel en vormen ongeveer 5 tot 10% van de totale populatie van gliacellen. Deze cellen zijn verantwoordelijk voor de productie van de myelineschede, die essentieel is niet alleen voor de snelle en efficiënte geleiding van elektrische impulsen langs de axonen, maar ook voor het behoud van de integriteit van de axonen. Oligodendrocyten ontstaan uit oligodendrocyt-voorlopercellen die zich net voor en na de geboorte vermenigvuldigen en differentiëren, onder een zeer gereguleerd programma. Zowel oligodendrocyten als hun voorlopers zijn zeer vatbaar voor letsel door verschillende mechanismen, waaronder excitotoxische schade, oxidatieve stress en ontstekingsreacties. In deze review zullen we niet alleen enkele belangrijke aspecten van de ontwikkeling van oligodendrocyten en regulerende mechanismen die bij dit proces betrokken zijn behandelen, maar ook enkele van de belangrijkste trajecten van letsel bespreken die geassocieerd zijn met oligodendrogenese. Bovendien zullen we ook enkele neurologische aandoeningen bespreken die zich gedurende het leven voordoen en die beperkingen in de functie van oligodendrocyten en myelinisatie tijdens de neuro-ontwikkeling veroorzaken, zoals periventriculaire leukomalacie, hypoxie/ischemie en hyperbilirubinemie, die op hun beurt de opkomst van neurologische en neurodegeneratieve ziekten zoals schizofrenie, multiple sclerose en de ziekte van Alzheimer kunnen versterken [4].
Oligodendrocyten zijn de myeliniserende cellen van het centrale zenuwstelsel en vormen ongeveer 5 tot 10% van de totale populatie van gliacellen. Deze cellen zijn verantwoordelijk voor de productie van de myelineschede, die essentieel is niet alleen voor de snelle en efficiënte geleiding van elektrische impulsen langs de axonen, maar ook voor het behoud van de integriteit van de axonen. Oligodendrocyten ontstaan uit oligodendrocyt-voorlopercellen die zich net voor en na de geboorte vermenigvuldigen en differentiëren, onder een zeer gereguleerd programma. Zowel oligodendrocyten als hun voorlopers zijn zeer vatbaar voor letsel door verschillende mechanismen, waaronder excitotoxische schade, oxidatieve stress en ontstekingsreacties. In deze review zullen we niet alleen enkele belangrijke aspecten van de ontwikkeling van oligodendrocyten en regulerende mechanismen die bij dit proces betrokken zijn behandelen, maar ook enkele van de belangrijkste trajecten van letsel bespreken die geassocieerd zijn met oligodendrogenese. Bovendien zullen we ook enkele neurologische aandoeningen bespreken die zich gedurende het leven voordoen en die beperkingen in de functie van oligodendrocyten en myelinisatie tijdens de neuro-ontwikkeling veroorzaken, zoals periventriculaire leukomalacie, hypoxie/ischemie en hyperbilirubinemie, die op hun beurt de opkomst van neurologische en neurodegeneratieve ziekten zoals schizofrenie, multiple sclerose en de ziekte van Alzheimer kunnen versterken [4].
Het doel van deze studie is om manieren te vinden om beschadigde zenuwvezels, met name in ziekten zoals multiple sclerose, te herstellen. Dit vereist het activeren van het myelinisatieprogramma in oligodendrocyt-voorlopercellen (OPC's). De controle over hoe deze voorlopercellen zich ontwikkelen tot volwaardige myelineproducerende cellen tijdens het herstelproces is nog niet goed begrepen.
De onderzoekers hebben getest of bepaalde stoffen die werken tegen een eiwit genaamd LINGO-1 kunnen helpen bij het bevorderen van myelinisatie in laboratoriumexperimenten (in vitro) en bij het herstel van myeline in het zenuwstelsel van knaagdieren (in vivo).
De resultaten laten zien dat in laboratoriumomstandigheden behandeling met stoffen die LINGO-1 blokkeren, de ontwikkeling van OPC's en myelinisatie bevorderde. Ook bleek dat in levende knaagdieren, waar demyelinisatie (verlies van de beschermende myelineschede rond zenuwvezels) was opgewekt door stoffen als lysophosphatidylcholine of cuprizone, het herstel van myeline versneld werd door behandeling met LINGO-1-antagonisten. Dit herstel was ook geassocieerd met verbeterde ontwikkeling van OPC's en een betere geleiding van zenuwimpulsen.
In eenvoudige bewoordingen betekent dit dat het blokkeren van LINGO-1 lijkt te helpen bij het herstellen van beschadigde zenuwvezels door de ontwikkeling van bepaalde voorlopercellen te bevorderen, waardoor de beschermende myelineschede sneller wordt hersteld [3].
Remyelinisatie stelt de axon in staat actiepotentialen over te dragen via zoutatorische geleiding, een eigenschap die verloren gaat bij demyelinisatie. Verschillende lijnen van bewijs geven aan dat remyelinisatie een belangrijke bijdrage levert aan het herstel van functionele tekorten die ontstaan door demyelinisatie en mogelijk ook een rol speelt bij het beschermen van axonen tegen de atrofie waaraan ze kwetsbaar zijn bij inflammatoire demyeliniserende ziekte. Dit hoofdstuk bespreekt de morfologische kenmerken van remyelinisatie. Een kenmerkend aspect van de morfologie van remyelinisatie is dat de nieuwe myelineschede onveranderlijk dunner en korter is dan verwacht zou worden voor de diameter van de axon. Dit hoofdstuk beschrijft ook remyelinisatie bij klinische ziekten en in experimentele modellen. Het succes van remyelinisatie hangt af van blootstelling van oligodendrocyten voorlopercellen (OPC's) aan de juiste omgevingssignalen die zowel de wervings- als differentiefasen bemiddelen. Regulering van de proliferatie en migratie van OPC's is een van de meest bestudeerde gebieden van de oligodendrocytenbiologie, hoewel doorgaans in de context van ontwikkeling. Bovendien bespreekt het hoofdstuk de remyelinisatie van het CZS door Schwann-cellen en de vooruitzichten voor therapeutische bevordering van remyelinisatie.
Myeline en Lion's Mane
Myeline, een essentiële component van het zenuwstelsel, speelt een cruciale rol in de efficiënte werking van neurale signalen. Schade aan myeline wordt geassocieerd met neurologische aandoeningen zoals multiple sclerose (MS). De laatste jaren is de medicinale paddenstoel Lion’s Mane (Hericium erinaceus) in de schijnwerpers gekomen vanwege zijn vermeende vermogen om myelineherstel en zenuwregeneratie te bevorderen. In dit artikel verkennen we de wetenschap achter myeline, de eigenschappen van Lion’s Mane en het potentieel van deze paddenstoel bij myelineherstel.
Wat is Myeline?
Myeline is een vettige substantie die de axonen van zenuwcellen omhult, vergelijkbaar met de isolatielaag rond elektriciteitskabels. Deze laag zorgt ervoor dat elektrische signalen snel en accuraat worden doorgegeven. Myeline wordt geproduceerd door gespecialiseerde cellen: oligodendrocyten in het centrale zenuwstelsel (CZS) en Schwann-cellen in het perifere zenuwstelsel (PZS). Schade aan myeline kan leiden tot vertraagde of verstoorde signaaloverdracht, met symptomen zoals spierzwakte, coördinatieproblemen en cognitieve achteruitgang.
Myelineherstel en Nerve Growth Factor (NGF)
Nerve Growth Factor (NGF) is een eiwit dat essentieel is voor het onderhoud, de groei en de overleving van zenuwcellen. NGF speelt ook een rol in de regeneratie van myeline. Het stimuleren van NGF-productie is daarom een veelbelovende strategie om myelineherstel te bevorderen. Hoewel farmacologische interventies in ontwikkeling zijn, wordt ook gekeken naar natuurlijke middelen zoals Lion’s Mane.
Lion’s Mane: Een Medicinale Paddenstoel
Hericium erinaceus, beter bekend als Lion’s Mane, is een paddenstoel die al eeuwenlang wordt gebruikt in de traditionele Chinese en Japanse geneeskunde. Moderne wetenschappelijke studies hebben aangetoond dat Lion’s Mane bioactieve verbindingen bevat, zoals hericenonen en erinacines. Deze stoffen kunnen de productie van NGF stimuleren en hebben neuroprotectieve eigenschappen.
Wetenschappelijk Bewijs
NGF-Stimulatie
Een studie gepubliceerd in het Journal of Agricultural and Food Chemistry (2005) toonde aan dat erinacines in Lion’s Mane de synthese van NGF kunnen verhogen in zenuwcellen. Dit suggereert dat de paddenstoel kan bijdragen aan het herstel van beschadigd zenuwweefsel.
Neuroprotectie
Een onderzoek uit 2011 in Biomedical Research rapporteerde dat ratten die Lion’s Mane-supplementen kregen, verbeteringen vertoonden in zenuwfunctie na zenuwbeschadiging. De onderzoekers concludeerden dat de paddenstoel zowel neuroprotectieve als herstellende effecten had.
Toepassing bij Neurologische Aandoeningen
Klinische studies, zoals een gerandomiseerde gecontroleerde trial gepubliceerd in Phytotherapy Research (2009), hebben aangetoond dat Lion’s Mane kan helpen bij cognitieve achteruitgang bij oudere volwassenen met milde cognitieve stoornissen. Hoewel deze studies geen direct bewijs leveren voor myelineherstel, suggereren ze een gunstig effect op de gezondheid van het zenuwstelsel.
- Mogelijke Mechanismen Lion’s Mane lijkt te werken via meerdere mechanismen:
- Stimulatie van NGF: Bevordert regeneratie van beschadigde zenuwcellen en mogelijk myelineherstel.
- Anti-inflammatoire werking: Vermindert ontstekingen die myelinebeschadiging kunnen verergeren.
- Antioxidante eigenschappen: Beschermt zenuwcellen tegen oxidatieve stress.
Lion’s Mane is verkrijgbaar als supplement in verschillende vormen, waaronder capsules, poeders en extracten. De aanbevolen dosering varieert, maar ligt vaak tussen 500 en 3000 mg per dag. Het is belangrijk om een arts te raadplegen voordat men begint met supplementatie, vooral bij bestaande gezondheidsproblemen of medicatiegebruik.
Bronnen
- Kawagishi, H., et al. (2005). "Hericenones and erinacines: Stimulators of nerve growth factor (NGF)-synthesis from the mushroom Hericium erinaceum." Journal of Agricultural and Food Chemistry.
- Mori, K., et al. (2011). "Effects of Hericium erinaceus on Nerve Regeneration in Rats with Nerve Injury." Biomedical Research.
Mori, K., et al. (2009). "Improvement of mild cognitive impairment by oral intake of Hericium erinaceus." Phytotherapy Research.
BPC 157
BPC 157 zorgt ervoor dat de serotonine- en dopamine-systemen in je lichaam in balans blijven. Het reguleert deze belangrijke chemische systemen, waardoor ze op een evenwichtige manier functioneren. Dit heeft gunstige effecten op diverse gedragsstoornissen die anders zouden ontstaan door specifieke (over)stimulatie of beschadiging van neurotransmittersystemen. Daarnaast vertoont BPC 157 neuroprotectieve eigenschappen, zoals het beschermen van somatosensorische neuronen, regeneratie van perifere zenuwen na doorsnijding, en het tegengaan van de voortgang na traumatisch hersenletsel. In experimenten met ratten met ruggenmergcompressie en staartverlamming blijkt BPC 157 ook effectief in het voorkomen van axonale en neuronale necrose, demyelinisatie, cystevorming en het herstellen van de staartfunctie op zowel korte als lange termijn. Verder zijn er positieve resultaten waargenomen bij verminderde letselverschijnselen in het maagdarmkanaal, de lever en de bloedvaten na overdosering met NSAID's, insuline, of cuprizone encefalopathieën [3, 4, 5, 6, 7, 8, 9, 10].

Remyelinisatie is herstel in het volwassen centrale zenuwstelsel (CZS), waarbij nieuwe myelineschedes worden gegenereerd rond gedemyeliniseerde axonen. Dit volgt op het pathologisch verlies van myeline, zoals zich voordoet bij demyeliniserende ziekten, met name multiple sclerose (MS). Remyelinisatie werd gedocumenteerd in vroege morfologische beschrijvingen van hersenen van MS-patiënten (Marburg, 1906). Plekken in vers geïsoleerd CZS-weefsel zijn gemakkelijk te identificeren als aparte, verkleurde gebieden waar myeline verloren is gegaan. Naast dergelijke klassieke plekken worden scherp afgebakende gebieden met verminderde myelinedichtheid waargenomen, herkenbaar aan gelijkmatig verdeelde, lichtgekleurde myelinekleuring die de Markschattenherde of schaduwplekken vertegenwoordigen (Schlesinger, 1909) (Figuur 1). Hoewel dergelijke observaties aanvankelijk werden toegeschreven aan onvolledige demyelinisatie (door voortdurende evolutie van laesies), waren er eerder suggesties dat een proces van herstel kon volgen op schade aan myeline (Marburg, 1906). Ondanks dit werd de bevestiging dat spontane remyelinisatie kon volgen op verlies van myeline pas geleverd in 1961, toen een baanbrekende ultrastructurele studie (met behulp van de methode van cerebrospinale vloeistof barbotage om demyelinisatie op te wekken) duidelijk aantoonde dat gedemyeliniseerde axonen in het ruggenmerg van de volwassen kat nieuwe myelineschedes kunnen verwerven (Bunge et al., 1961). Dit volgde op hun eerdere observaties uit lichtmicroscopische studies dat myeline opnieuw verschijnt op het moment dat dieren herstellen van gedeeltelijke verlamming (Bunge 1958, Bunge 1957). Het idee dat de dunne myelineschijven waargenomen in gedemyeliniseerde laesies gebieden van spontane remyelinisatie zouden kunnen vertegenwoordigen, kwam voort uit een ultrastructurele studie van MS-plekken (Perier en Gregoire, 1965). Bovendien bewezen andere studies dat remyelinisatie niet alleen structureel herstel veroorzaakte, maar ook axonen in staat stelde om geleidingseigenschappen (Smith et al., 1979) en neurologische functie die verloren was gegaan als gevolg van demyelinisatie, terug te krijgen (Jeffery en Blakemore, 1997) [11].
Tekenen en symptomen van MS variëren sterk tussen patiënten en zijn afhankelijk van de locatie en ernst van de schade aan zenuwvezels in het centrale zenuwstelsel. Sommige mensen met ernstige MS kunnen het vermogen verliezen om zelfstandig te lopen of helemaal te bewegen. Anderen kunnen lange perioden van remissie ervaren zonder nieuwe symptomen, afhankelijk van het type MS dat ze hebben [12].
Symptomen
Veelvoorkomende symptomen zijn onder andere:
- Gevoelloosheid of zwakte in één of meer ledematen, die meestal aan één kant van je lichaam tegelijk optreedt
- Prikkelingen
- Elektrische schok sensaties die optreden bij bepaalde nekbewegingen, vooral bij het voorover buigen van de nek (Lhermitte-teken)
- Gebrek aan coördinatie
- Onstabiele gang of onvermogen om te lopen
- Gedeeltelijk of volledig verlies van het gezichtsvermogen, meestal in één oog tegelijk, vaak met pijn tijdens oogbewegingen
- Langdurige dubbelzien
- Wazig zien
- Duizeligheid
- Problemen met seksuele, darm- en blaasfunctie
- Vermoeidheid
- Onduidelijke spraak
- Cognitieve problemen
- Stemmingsstoornissen
Bronnen
- Multiple sclerosis - Symptoms and causes - Mayo Clinic https://www.mayoclinic.org/diseases-conditions/multiple-sclerosis/symptoms-causes/syc-20350269
- Multiple Sclerosis (MS) https://www.hopkinsmedicine.org/health/conditions-and-diseases/multiple-sclerosis-ms#:~:text=Multiple%20sclerosis%20(MS)%20is%20a%20chronic%20disease%20of%20the%20central,trouble%20walking%2C%20and%20tingling%20feelings.
- Brain-gut Axis and Pentadecapeptide BPC 157: Theoretical and Practical Implications https://pubmed.ncbi.nlm.nih.gov/27138887/
- Brain-gut Axis and Pentadecapeptide BPC 157: Theoretical and Practical Implications https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5333585/
- Stable gastric pentadecapeptide BPC 157 can improve the healing course of spinal cord injury and lead to functional recovery in rats https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6604284/
- Stable Gastric Pentadecapeptide BPC 157 and Striated, Smooth, and Heart Muscle https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9775659/
- The Brain-gut Axis-where are we now and how can we Modulate these Connections? https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8719292/
- Natural Therapies to Support Myelin Health https://restorativemedicine.org/digest/natural-therapies-support-myelin-health/
- Placebo-controlled phase 3 study of oral BG-12 or glatiramer in multiple sclerosis https://pubmed.ncbi.nlm.nih.gov/22992072/
- Placebo-controlled phase 3 study of oral BG-12 for relapsing multiple sclerosis https://pubmed.ncbi.nlm.nih.gov/22992073/
- Remyelination In Multiple Sclerosis https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7112255/
- Multiple sclerosis https://www.mayoclinic.org/diseases-conditions/multiple-sclerosis/symptoms-causes/syc-20350269
- Is BPC 157 the Future of Healing?
Brieven
Fase II van het ontwikkelingstraject
Na succesvolle tests op 16 personen maakt BPC 157 de overgang naar Fase II van het ontwikkelingstraject, gericht op de behandeling van multiple sclerose (MS). Deze fase vertegenwoordigt een belangrijke stap in de verdere evaluatie en ontwikkeling van BPC 157 als een veelbelovende therapie voor deze neurologische aandoening.
Wij nodigen geïnteresseerde deelnemers uit om deel te nemen aan deze fase van het onderzoek. Als u zich wilt aanmelden voor de klinische proeven of meer informatie wenst, verwijzen wij u graag naar onze contactpagina.
Multiple sclerose (MS) is een potentieel invaliderende ziekte van de hersenen en het ruggenmerg (centraal zenuwstelsel). Bij MS valt het immuunsysteem de beschermende laag (myeline) aan die zenuwvezels bedekt, wat communicatieproblemen veroorzaakt tussen je hersenen en de rest van je lichaam. Uiteindelijk kan de ziekte permanente schade of achteruitgang van de zenuwvezels veroorzaken [12].
In MS valt het immuunsysteem de beschermende schede (myeline) aan die zenuwvezels bedekt, wat communicatieproblemen veroorzaakt tussen je hersenen en de rest van je lichaam. Uiteindelijk kan de ziekte permanente schade of achteruitgang van de zenuwvezels veroorzaken [1]. Myeline is het vettige weefsel dat zenuwvezels omringt en beschermt. Bij MS wordt de myeline op veel plaatsen vernietigd. Dit verlies van myeline vormt littekenweefsel, ook wel sclerose genoemd. Deze gebieden worden ook wel plaques of laesies genoemd. Wanneer de zenuwen op deze manier beschadigd zijn, kunnen ze geen elektrische impulsen meer geleiden van en naar de hersenen [2].




